1.- Clasificación de los materiales metálicos:
- Los materiales metálicos los clasificaremos en:
- Estaño
- Color blanco azulado brillante
- Blando
- Inoxidable
- Se aplica en soldadura de elementos eléctricos de baja tensión y en soldadura de tubos de calefacción
- Cinc
- Color blanco
- Muy resistente a la corrosión y oxidación
- Se aplica en el recubrimiento de tejados, canalones y tubos
- Magnesio
- Muy ligero
- Muy caro
- Reacciona mal con el oxigeno en su forma liquida
- Se aplica en componentes aeroespaciales y se usa en pirotecnia y explosivos.
- Titanio
- Muy caro
- Resistente a la corrosión
- Muy buena resistencia mecánica
- Se utiliza como componente medico debido a su biocompatibilidad
- Se aplica en implantes biomecánicos, motores de turbo reacción y estructuras de aeronaves
- Aleaciones a través de estos:
- Latón:
- Cobre y Cinc
- De un 5% a un 40% de Zn
- Color amarillo
- Muy dúctil y maleable
- Se aplica a cerraduras, radiadores, accesorios de fontanería...
- Bronce
- Cobre y estaño
- Un 10% de Sn
- Color amarillo oscuro
- Resistente a la corrosión
- Se aplica en engranajes, cojinetes, estatuas, monumentos...
- Propiedades:
- Conducen bien el calor y electricidad
- Sólidos a temperatura ambiente (excepto el mercurio)
- Tienen un punto de fusión (paso del solido al liquido)
- Son maleables y dúctiles
- Oro, plata y bronce los mas dúctiles
- Ductilidad:
- Propiedad por la que algunos metales y aleaciones pueden estirarse sin romperse permitiendo obtener hilo y alambre
- Maleabilidad:
- Propiedad por la que los cuerpos pueden ser labrados por deformación
2.- ENLACE METÁLICO:
- Es un enlace químico que mantiene unidos los átomos de los metales entre si. Estos átomos se agrupan de forma muy cercana unos a otros, lo que hace que su estructura sea muy compacta.
- En este tipo de estructura cada átomo metálico está dividido por otros doce átomos (seis en el mismo plano, tres por encima y tres por debajo).
- El enlace metálico es característico de los elementos metálicos. Es un enlace fuerte, primario, que se forma entre elementos de la misma especie. Al estar los átomos tan cercanos unos de otros, interaccionan sus núcleos junto con sus nubes electrónicas, empaquetándose en las tres dimensiones, por lo que quedan los núcleos rodeados de tales nubes. Estos electrones libres son los responsables de que los metales presenten una elevada conductividad eléctrica y térmica, ya que estos se pueden mover con facilidad si se ponen en contacto con una fuente eléctrica.
- Enlace esplicativo
3.- CARACTERÍSTICAS Y PROPIEDADES FÍSICAS Y QUÍMICAS DE LOS MATERIALES METÁLICOS
- Dentro de la clasificación de los materiales encontramos la siguiente tabla resumen, la cual abarca mas de lo que el propio enunciado pide, pero que es bueno mostrar que no solo tienen unas propiedades químicas y físicas los materiales, si no que existen otras dos ramas diferentes para la clasificación total de dichos elementos.
- Según las propiedades físico-químicas de los materiales, estos cambian su manera de comportarse y de reaccionar cuando se encuentran en ambientes y situaciones especiales que pueden y suelen presentarse en su proceso de fabricación.
- Dentro de las propiedades físicas, destacaremos las mas importantes:
- La masa volúmica
- Es diferente para cada material
- Libro explicativo
- Dilatación térmica
- Es el aumento, longitud, volumen y alguna que otra dimensión métrica que sufre un cuerpo debido al aumento de temperatura que se le provoca
- En esta web, se explica muy claro en que se vasa la dilatación térmica, y muestra dentro de ella el coeficiente de dilatación que muestro en el blog a continuación:
- Aluminio 0,000024
Bronce 0,000018
Hormigón 0,000018
Cobre 0,000017
Fundición de hierro 0,000012
Acero 0,000013
Platino 0,000009
Vidrio térmico 0,000003
Vidrio comercial 0 000011
Cuarzo fundido 0,0000005
Invar (aleación) 0,0000009
Roble, a lo largo de fibra 0,000005
Roble, a lo ancho de fibra 0,000054
Caucho duro 0,000080 - Punto de fusión o solidificación
- Aunque lo parezca, no es lo mismo. El punto de fusión es la temperatura a la cual se encuentra el equilibrio de fases, de solido a liquido. Mientras que la solidificación es un proceso físico que consiste en un cambio de estado de la materia de liquido a solido debido a la disminución de la temperatura que se le esta aplicando.
- En este articulo de la revista investigación y ciencia lo explican muy bien.
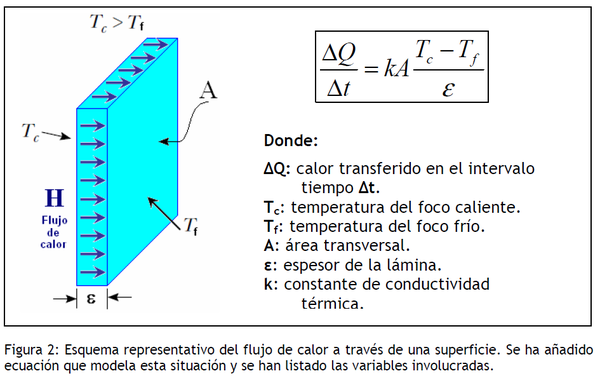
- Conductividad térmica
- Es una propiedad física de los materiales que mide la capacidad de conducción del calor, es la capacidad de transferir energía cinética de sus moléculas a otras moléculas adyacentes.
4 - ESTRUCTURA INTERNA DE LOS MATERIALES METÁLICOS
- Los materiales están formados por varios elementos
- Molécula
- Es la mínima proporción de la materia que conserva las propiedades de un material
- Átomo
- Es la unidad de materia mas pequeña de un elemento químico que mantiene su identidad o propiedades y que no es posible dividir salvo por procesos químicos.
- Pero lo que le da sus propiedades es su estructura cristalina, que se divide en 7 sistemas cristalinos y 14 retículos especiales.
- Cristales metálicos
- Su estructura es mas simple, ya que cada punto reticular del cristal esta ocupado por un átomo del mismo metal
- Se caracterizan por tener pocos electrones
- Están cargados primitivamente
- Características:
- Buena conductividad eléctrica
- Buena conductividad térmica
- Alta resistencia mecánica
- Rigidez
- Ductilidad
- Trabajo explicativo sobre la estructura de los materiales
5 - PUREZA Y ALEACIONES
- La pureza es la ausencia de suciedad, impurezas y otros elementos que pueden contaminar los metales. Son aquellos que carecen de inperfección.
- Los metales puros son los que se encuentran en forma natural o "pura" dentro de la naturaleza, aunque en general los metales se asocian con compuestos como el oxigeno (O) o con un metal como son los siguientes casos:
- Cloro (Cl)
- Azufre (S)
- Carbono (C)
- Los metales nativos o puros son:
- Plata (Ag)
- Oro (Au)
- Cobre (Cu)
- Platino (Pt)
- En ocasiones se utilizan aleaciones metálicas ya que combinando distintos metales se pueden conseguir mejores propiedades.Debido al elevado coste de algunos metales utilizados para evitar la corrosión, se han desarrollado algunos métodos para mantener la resistencia a la corrosión más económicamente. El acero al carbono suele utilizarse para proteger estructuras, tuberías o recipientes. Para mejorar su resistencia se les añade cromo. El Incoloy 825 es muy resistente a la corrosión por la presencia del ion cloruro. Es una aleación con base de níquel.Los aceros inoxidables son aleaciones con base de acero y con un alto contenido en cromo. También suele añadirse otros elementos como níquel para aumentar más su resistencia a la corrosión.
- MÉTODOS DE PROTECCIÓN
- Existen diversos métodos para la protección contra la corrosión:
- Métodos modificando el medio
- Métodos modificando el diseño
- Métodos por recubrimientos protectores
- Métodos modificando el metal
- Métodos por planificación electroquímica
- Métodos modificando el medio
- Son clásicos, dentro de estos métodos, los siguientes:
- La deshumidificación del aire
- La desaireación del agua
- La adición de inhibidores de corrosión
- En un buen número de procesos de corrosión electroquímica se establece la intervención del agua (Electrolito) y del oxígeno (reactivo catódico). La eliminación de uno u otro de estos elementos, necesarios para la corrosión, conlleva la supresión del proceso corrosivo. Los inhibidores se utilizan principalmente en sistemas que utilizan un volumen constante de disolución del metal.
- Se clasifican según su composición química en:
- Orgánicos
- Inorgánicos
- Según su actuación:
- Anódicos
- Catódicos
- De adsorción
- Según circunstancias de su aplicación:
- De decapado
- Para soluciones neutras
- En fase vapor
- Métodos modificando el diseño
- Hay factores que se pueden evitar con un diseño adecuado del equipo o estructura metálica. Como normas básicas se debe evitar el contacto directo entre metales de muy distintas características Electroquímicas.
- Métodos por recubrimientos protectores
- Hacen de barrera entre el metal y el agente corrosivo.Se clasifican en:
- Orgánicos
- Inorgánicos
- Metálicos
- Por películas pasivas
6 - BREVE HISTORIA DE LA HUMANIDAD RELACIONADA CON LOS MATERIALES METÁLICOS.
Al igual que la escritura, el descubrimiento de losmetales y la forma de procesarlos, marcan la división entre la edad de piedra y el inicio de las civilizaciones en la llamada“Edad de los metales”. En la edad de cobre(4400 – 3800 a. C.) aparece la metalurgia y minería, comenzado a trabajarse el cobre y el oro, para fabricar armas rústicas como punzones, hachas, puñales, punta de flechas, y ornamentos como anillos y brazaletes. Tras el descubrimiento del bronce, una aleación de nueve partes de cobre y una de estaño se inicia la edad de bronce (a partir del 2800 a. C.). Este material ofrece la posibilidad de trabajar con mayor facilidad y se pueden producir utensilios mucho más duros y trabajos ornamentales más finos. La última era de los metales está representada por la edad de hierro (1300 a. C.) y es la etapa previa a la creación del imperio romano . La mayor ventaja del hierro sobre el bronce es que las vetas eran mucho más abundante s y por tanto era un material más económico. Además, no es necesaria aleación alguna y constituye un material admirable para la fabricación de sierras, hachas, a zuelas y clavos. Sin embargo, es un material más difícil de trabajar y de temperatura de fundición más elevada, por eso se explica que su uso haya demorado tanto. La producción de hierro, sin embargo, no fue exclusiva del occidente, pues en China también hay registros de su uso a partir del año 600 a. C. Y de hecho, esta nación fue la única que pudo trabajar el hierro en molde. El trabajo en hierro promovió el perfeccionamiento de técnicas metalúrgicas, el desarrollo de la forja y la herrería para la construcción de armas y herramientas de mayor dureza, calidad y duración.
Link de donde he sacado la información
7 - EXTRACCIÓN, PRODUCCION Y RECICLADO DE MATERIALES METÁLICOS
- Los materiales metalicos, antes de ser tal material son minerales, los cuales contienen ese metal que se extrae. La forma tradicional es moler los minerales y disolverlos con cianuro, el problema es que el uso de ese material lo que origina es que no se disuelva bien y origina gases toxicos.
8 - OXIDACIÓN Y CORROSIÓN
- Los materiales están expuestos continuamente a los más diversos ambientes de interacción material-ambiente provoca, en muchos casos, la pérdida o deterioro de las propiedades físicas del material. Los mecanismos de deterioro son diferentes según se trate de materiales metálicos, cerámicos o polímeros (plásticos). Así, en el hierro, en presencia de la humedad y del aire, se transforma en óxido, y si el ataque continúa acaba destruyéndose del todo. Desde el punto de vista económico, la corrosión ocasiona pérdidas muy elevadas. En los materiales metálicos, el proceso de deterioro se llama oxidación y corrosión.
- Oxidación directa:
- Resulta de la combinación de los átomos metálicos con los de la sustancia agresiva
- Corrosión electroquímica o corrosión en líquidos.
- En este caso, el metal es atacado por un agente corrosivo en presencia de un un electrolito
Enlace sobre Oxidacion y corrosion
Presentacion sobre oxidación y corrosión
Biblio:
Libro sobre carrocería
Libro sobre la clasificación de los materiales
Blog de materiales de gran pureza
Enlace 1
Enlace 2
Enlace 3
Enlace 4









.jpg/200px-Esfalerita_Cartagena_(Murcia).jpg)

















No hay comentarios:
Publicar un comentario